概要
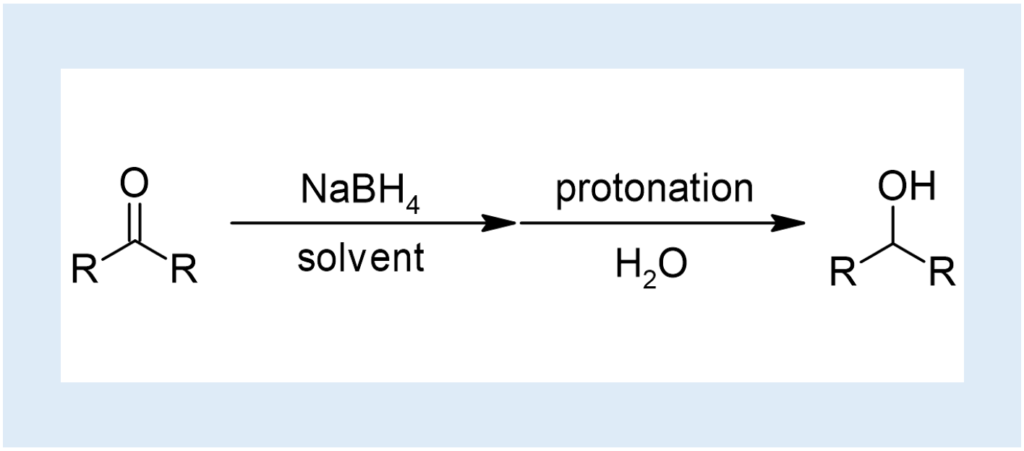
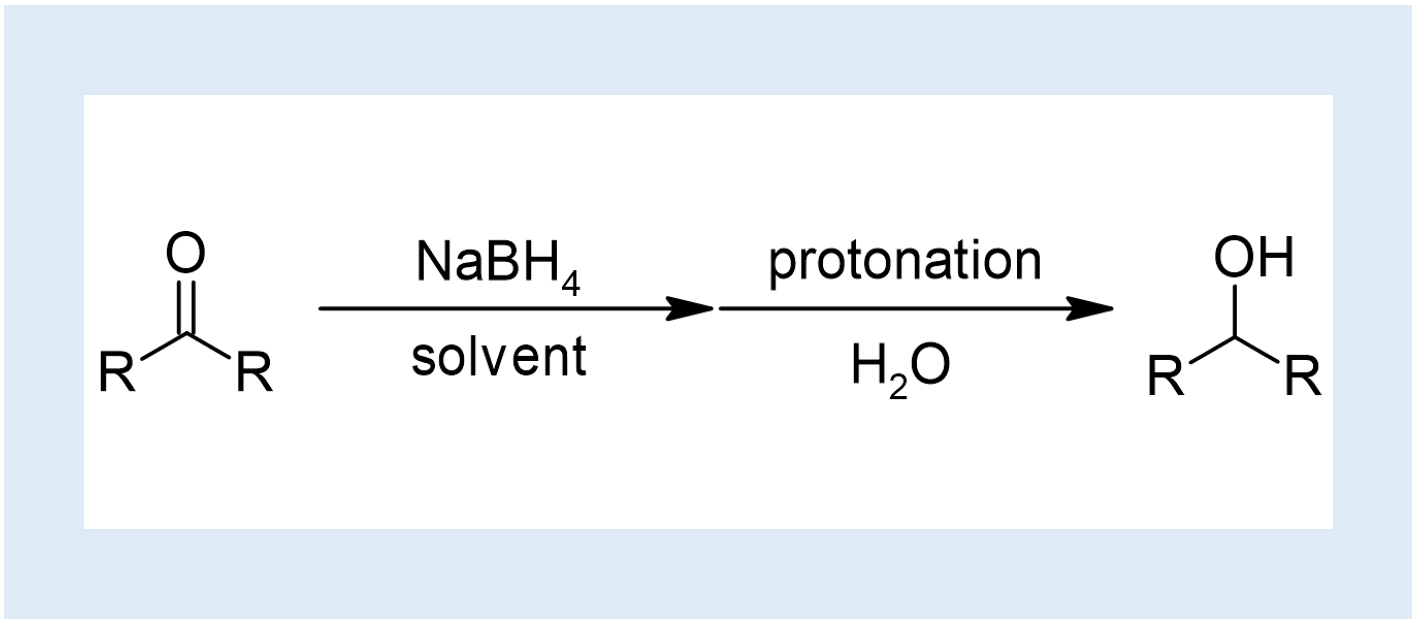
アルデヒドやケトンをOHへと還元する手法の一つ。
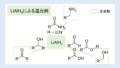
還元力は水素化アルミニウムリチウム(LiAlH4)より弱く、安定で扱いが容易である。
エステル、カルボン酸、アミドは通常還元できないため、アルデヒドやケトンを選択的に還元することが可能である。
反応機構
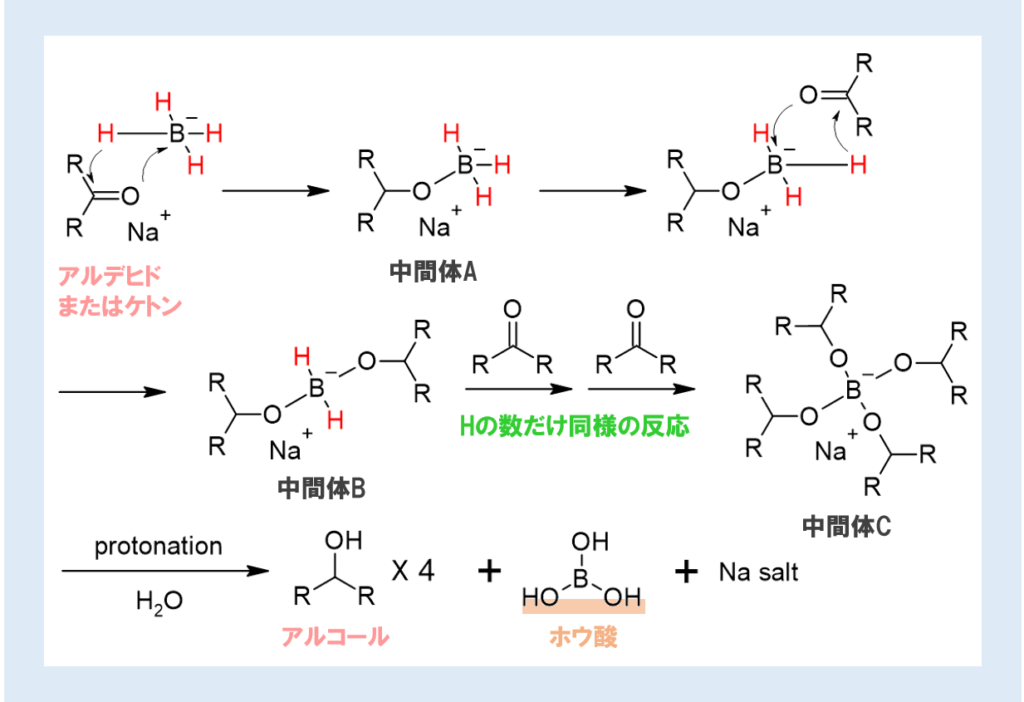
まず、アルデヒドまたはケトンに対しBH4–のヒドリドが求核付加するとともに、これによって電子を得たOがBH3に求核付加することで中間体Aが生じる。
次に、中間体Aのヒドリドが同様にアルデヒドまたはケトンに求核付加するとともに、これによって電子を得たOが中間体Aに求核付加することで中間体Bが生じる。
同様の反応が残ったヒドリド(赤色で表示したH)の数だけ行われ、中間体Cが生じる
これにプロトン付加して加水分解することで、目的のOH4分子と、副生成物としてホウ酸とナトリウム塩を得る。
上に示した通り、NaBH4 1分子から4分子の目的物を得ることができるが、通常NaBH4は過剰量で反応が行われる。
NaBH4 1分子が1分子の原料と反応する場合を例として、以下でNaBH4過剰量での機構を解説する。
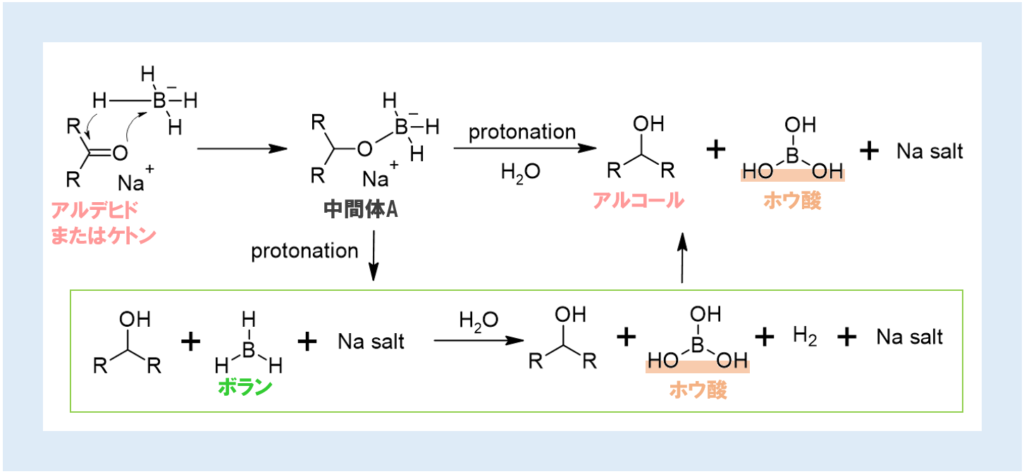
アルデヒドまたはケトンは、同様にして中間体Aとなる。
その後、プロトン付加によって生じたボランはすぐに加水分解され、ホウ酸と水素が生じる(緑の枠内)。
結果、反応をまとめると上段の式となる(水素は系内に残らないため省略)。
このようにNaBH4過剰量では、加水分解によりボラン化合物からホウ酸と水素が生じる。
近年における使用例
①
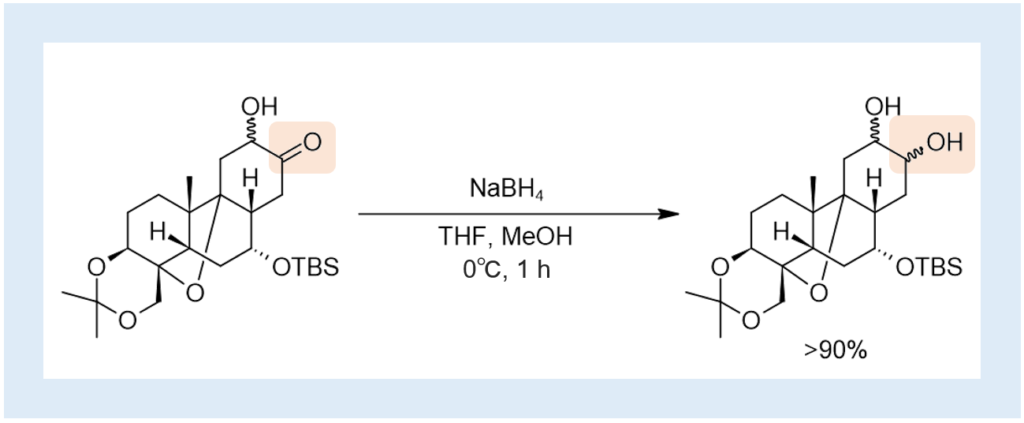
0℃に氷冷したTHF 5mlと、脱水MeOH 7.5 mlの混合溶液に、ケトン 448 mg(およそ1.03 mmolを未精製で使用している。不純物の含有量は不明。)とNaBH4 33mg (0.87 mmol)を加え、アルゴン下で1時間攪拌。TLCで原料の消失を確認した後、NH4ClaqをpH7~8まで加えた。揮発物を除去した後、CH2Cl2で抽出し、カラムで精製して目的物を得た。(>90%、複数ステップの最終物)
②
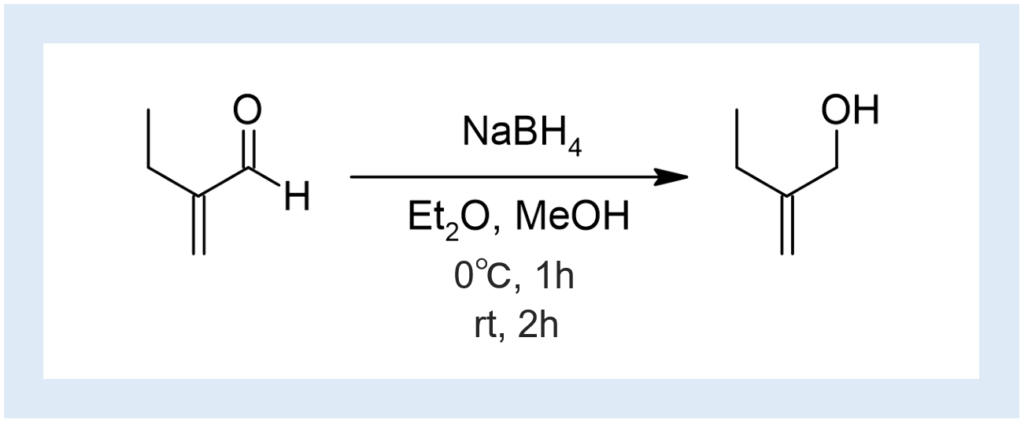
0℃に氷冷したEt2O 85 mlとMeOH 20 mlの混合溶液に、アルデヒド 12.3 ml (0.190 mol)とNaBH4 4.80 g (0.127 mol)を加えて1時間攪拌した後、室温で2時間攪拌した。反応後、水 140 mlとEt2O 70 mlを加え、水層をEt2O 70 ml×3で抽出し、MgSO4で脱水した後、溶媒留去した。(複数ステップの途中のため収率表記なし)
※いずれもクエンチでの水素の発生に注意
試薬価格
※下記は一例です。販売会社、時期、グレードなどによって価格は異なります。
NaBH4 : 100 g / 5000円程度 (CAS:16940-66-2)
参考文献
基本文献
Tetrahedron Lett. 1983, 24, 1015-1018.
使用例
①Org. Lett. 2017, 19, 19, 5150–5153.
②Org. Lett. 2016, 18, 5, 1032–1035.